
УДК 576.8:573.6.086.83:579.842.1:579.841.1:578.825.1
DOI 10.33861/2071-8020-2026-1-32-36
Оригинальное эмпирическое исследование
Романова Н. Н. Филиал по пресноводному рыбному хозяйству государственного научного центра Российской Федерации
федерального государственного бюджетного научного учреждения «Всероссийский научноисследовательский институт
рыбного хозяйства и океанографии» Московская область, п. Рыбное / Дмитровский рыбохозяйственный технологический
институт (филиал) федерального государственного бюджетного образовательного учреждения высшего образования
«Астраханский государственный технический университет», Московская область, п. Рыбное /
Федеральное государственное бюджетное образовательное учреждение высшего образования «Московская
государственная академия ветеринарной медицины и биотехнологии – МВА имени К.И. Скрябина», г. Москва
Токарева С. Б., Щелкунова Ю. П. Филиал по пресноводному рыбному хозяйству государственного научного центра Российской
Федерации федерального государственного бюджетного научного учреждения «Всероссийский научно-исследовательский
институт рыбного хозяйства и океанографии» Московская область, п. Рыбное
Аннотация. Циркуляция инфекций на рыбоводных предприятиях наносит серьезный урон поголовью, что вызывает высокий спрос у ихтиопатологов на разработку экспресс-диагностикумов и таких препаратов, как вакцины и бактериофаги.
Цель работы – формирование коллекции изолятов/штаммов бактерий и вирусов для системы охраны здоровья объектов аквакультуры.
Материалы и методы исследований. Коллекция формируется из полевых изолятов патогенных бактерий и вирусов, выделяемых от рыб с клиническими признаками заболеваний. Бактерии р. Aeromonas и р. Pseudomonas были выделены из внутренних органов рыб, накоплены на питательной среде эритритагар. Образцы консервировали криоконсервацией в жидком азоте при -196°С и замораживанием при -80°С. После хранения жизнеспособность бактерий оценивали путем посева на плотные питательные среды. Вирулентность аэромонад определяли на ДНК-тест агаре. Проверку видовых свойств и биохимической активности культур проводили на агаре Клиглера. Изоляты герпесвируса сибирского осетра накапливали в перевиваемых клеточных линиях осетрового происхождения: WSS-2, SSO-2. Для определения оптимальных условий хранения вируссодержаий материал консервировали с 10% фетальной телячьей сыворотки и сохраняли при +4°С; -18°С; -80°С. Титр вируса определяли методом Рида и Менча.
Результаты исследований и их обсуждение. Формирующаяся коллекция патогенов-возбудителей заболеваний рыб в лаборатории ихтиопатологии Филиала по пресноводному рыбному хозяйству ФГБНУ «ВНИРО» («ВНИИПРХ») включает 7 штаммов бактерий (Aeromonas hydrophila, A. veronii, A. salmonicida, A. eucrenophila, Pseudomonas sp. и 2 штамма Pseudomonas alcaligenes) и 6 изо-лятов герпесвируса (SbSHV). Штаммы бактерий выделены от лососевых, осетровых и карповых рыб в рыбоводных хозяйствах различного типа Центрального федерального округа РФ. В период хранения при режимах: криоконсервация в сжиженном азоте (t= -196°С), замораживание при ультранизкой температуре (t= -80°С) и охлаждение (t= +4 – +8°С) выявили сохранность высокой жизнеспособности бактерий (обильный и сливной рост – в 100% проб). Патогенность (ДНК-азная активность) штаммов аэромонад имела тенденцию к снижению, наиболее значимо уменьшилась у бактерии А. hydrophila. Изоляты SbSHV, находящиеся в коллекции, выделены в регионах РФ и ближнего зарубежья от разновозрастной молоди сибирского, русского осетров и их гибридов. По истечении 3 месяцев хранения изолятов в условиях разных температур инкубации (+4°С; -18°С; -80°С) выявили, что оптимальной являлась -80°С в условиях низкотемпературного морозильника.
Заключение. В коллекции заложено 6 изолятов герпесвируса, перед размещением на хранение у каждого изолята проверяли инфекционную активность, все варианты были с достаточно высоким титром от 4,1 до 6,1 lg ТЦД50/мл. По истечению 3 месяцев хранения герпесвируса сибирского осетра оптимальной являлась температура -80°С в условиях низкотемпературного морозильника. Ключевые слова: бактерии, род Aeromonas, род Pseudomonas, изоляты герпесвируса сибирского осетра, коллекция, хранение.
Возбудители инфекционных болезней циркулируют на многих предприятиях аквакультуры, что иногда приводит к значительным потерям рыбопосадочного материала и рыбной продукции. Большая заинтересованность
ихтиопатологов и рыбоводов существует в разработке экс-пресс-диагностикумов и лечебно-профилактических препаратов (вакцин и бактериофагов). В связи с этим актуальным становится формирование коллекции опасных возбудителей заболеваний рыб с описанием их биологических свойств.
Бактерии р. Aeromonas (аэромонады) являются сложной в таксономическом отношении группой. В мировой практике с помощью метода молекулярной гибридизации р. Aeromonas был выделен в самостоятельное семейство Aeromonadaceae [1]. В настоящий момент этот род объединяет в себе 45 видов [2]. Бактерии р. Aeromonas представлены клетками от прямых палочек с закругленными концами до сферических, 0,3-1,0?1,0-3,5 мкм, одиночные, в парах или коротких цепочках, грамотрицательные. Как правило, подвижные за счет единственного полярного жгутика, за исключением Aeromonas salmonicida, у которой жгутиков нет. Факультативные анаэробы. Хемоорганотрофы, обладающие дыхательным и бродильным типом метаболизма. Оптимальный диапазон температуры 22-28°С, большинство видов хорошо растет при температуре 37°С.
Бактерии р. Pseudomonas (псевдомонады) входит в семейство Pseudomonadaceae [3]. Это прямые или слегка изогнутые палочки размером 0,5-1,0?1,5-5,0 мкм, являются грамотрицательными, неферментирующими, в основном, подвижными и оксидазоположительными видами. Подвижность обеспечивается за счет одного или нескольких полярных жгутиков; в отдельных случаях могут быть неподвижными. Спор не образуют. Некоторые из них образуют капсулы и желто-зеленый флюоресцирующий пигмент.
Псевдомонады являются аэробами, большинство видов не растут в кислой среде (рН 4,5) и не нуждаются в органических факторах. Каталазоположительные, хеморганотрофы, некоторые виды – факультативные автотрофы, способные использовать в качестве источника энергии Н2 или СО [4]. Род Pseudomonas содержит более 140 видов, большинство из которых являются сапрофитами [5].
Аэромонады и псевдомонады являются обитателями водной среды, комбикормов и могут контаминировать рыбу, вызывая тяжело протекающие бактериальные заболевания: аэромоноз, фурункулез, эритродерматит, бактериальную геморрагическую септицемию, псевдомоноз. Факторами, способствующими развитию бактериозов, являются резкое повышение температуры воды, высокие плотности посадки, снижение резистентности организма рыб, неполноценное кормление, высокое содержание органических веществ в воде и другие нарушения гидрохимического режима, травматизация рыб.
Герпесвирус сибирского осетра относится к группе высоковирулентных герпесвирусов рода Ictalurivirus, семейства Alloherpesviridae, порядка Herpesvirales, является представителем группы герпесвирусов осетровых 2-го типа (AciHV-2), в генетическом отношении наиболее близок к канадскому изоляту герпесвируса тупорылого осетра Acipenser Brevirostrum [6, 7, 8]. Наряду с поражением кожных покровов, возбудитель вызывает системную, остропротекающую инфекцию, проявляющуюся дистрофическими и некротическими изменениями во внутренних органах. Клинически болезнь сопровождается появлением кровоизлияний на поверхности тела, нижней стороне рострума, в основании грудных и брюшных плавников, образованием на коже мелких бляшек гиперплазированного эпидермиса, гиперемией ануса, угнетением и отказом от корма.
Наиболее восприимчивыми к заболеванию являются сибирский и русский осетры, а также их гибриды. Менее восприимчивы стерлядь, бестер и их гибриды. Оптимальной температурой для развития заболевания и размножения вируса в органах и тканях чувствительных рыб является диапазон 11-19°С. Выше и ниже указанных пределов тяжесть течения инфекции снижается, как и вероятность выделения патогена от больных рыб. Оптимальными условиями культивирования вируса SbSHV in vitro является температура инкубации 15°С, при которой наблюдается его наибольшая инфекционная активность [9].
В Российской Федерации официальный банк патогенов-возбудителей заболеваний рыб отсутствует, но в отдельных лабораториях, в основном научно-исследовательских институтах, существуют собственные научно-исследовательские коллекции.
В лаборатории ихтиопатологии Филиала по пресноводному рыбному хозяйству ГНЦ РФ ФГБНУ «ВНИРО» (ВНИИПРХ) с 2023 года формируется коллекция патогенов для нужд рыбохозяйственной отрасли.
Формирование отраслевой научно-исследовательской коллекции бактерий и вирусов необходимо для сохранения внутривидового разнообразия возбудителей эпизоотически значимых видов для рыб. Накопление патогенных для рыб бактерий и вирусов, оптимизация процессов их сохранности, периодическая проверка жизнеспособности штаммов при различных условиях хранения и оценка их патогенности (вирулентности) является актуальной задачей при формировании коллекции.
Цель работы – формирование коллекции изолятов/штаммов бактерий и вирусов для системы охраны здоровья объектов аквакультуры.
Материалы и методы исследований. Коллекция формируется из полевых изолятов патогенных бактерий и вирусов, выделяемых от рыб с клиническими признаками заболеваний.
Бактерии р. Aeromonas и р. Pseudomonas были выделены из внутренних органов рыб, накоплены в нужном количестве на питательной среде эритритагар, перенесены в микропробирки Эппендорф с защитной средой (стерильный питательный бульон ГРМ – 90%, криопротектор ДМСО – 10%) – для замораживания и хранения при двух режимах: криоконсервация в сжиженном азоте при -196°С в сосуде Дьюара и при ультранизкой температуре -80°С в низкотемпературном морозильнике Bio Ultra UL570в. Для режима хранения в условиях охлаждения при +4 – +8°С бактерии были засеяны петлей в биологические пробирки в столбик стерильного полужидкого питательного агара и инкубированы до появления бактериального роста с последующим наслоением стерильного вазелинового масла на поверхность агара.
Для проверки жизнеспособности бактерий в течение хранения отбирали по 3 образца каждого вида и восстанавливали изоляты. С этой целью микропробирки с культурами штаммов после хранения в замороженном виде в жидком азоте (-196°C) и при ультранизкой температуре (-80°C) размораживали на водяной бане при температуре 37°С в течение 60-120 сек при осторожном встряхивании до полного оттаивания. Содержимое пробирок переносили количественно в чашки с питательным агаром (эритритагар), инокулят равномерно распределяли на поверхности агара. Чашки с инокулятом оставляли на столе до полного впитывания в агар, затем помещали на инкубирование в термостат при температуре 25-27°С. Культуры, хранившиеся при температуре +4 – +8°С, переносили из пробирок с полужидким агаром на чашки с питательным агаром (эритритагар), проводя поверхностный засев штрихом стерильной бактериологической петлей, и инкубировали при температуре 25-27°С. Результаты учитывали через 24-48 часов. Подсчет колоний проводили по их росту на питательных средах: единичный рост – от 1 до 10 КОЕ на чашке, умеренный рост – от 10 до 100 КОЕ на чашке, обильный рост – >100 КОЕ на чашке.
Вирулентность аэромонад определяли на ДНК-тест агаре [10]. Культуры, дающие зону деполимеризации до 2 мм – слабовирулентные, 2-4 мм – вирулентные, более 4 мм – высоковирулентные. Проверку видовых свойств и биохимической активности культур проводили на первично-дифференцирующем агаре Клиглера.
Изоляты герпесвируса сибирского осетра накапливали в перевиваемых клеточных линиях осетрового происхождения: WSS-2, SSO-2. Для культивирования вирусов и культур клеток использовали питательные среды 199, Игла МЕМ с двойным набором аминокислот и витаминов (Игла 2МЕМ) (ПанЭко, г. Москва), эмбриональную телячью сыворотку (Global Kang, Китай), растворы трипсина и версена, гентамицин.
Отбор и обработку патологического материала от рыб проводили в соответствии с требованиями национальных и международных нормативных документов по вирусологическому исследованию рыб [11, 12]. После обработки готовили четыре последовательных 10-кратных разведения материалов на питатель-
ной среде с добавлением антибиотиков (пенициллин, стрептомицин, амфотерицин), которыми инокулировали перевиваемые культуры клеток. Инокуляцию клеток производили одновременно с их посевом в 96-луночные пластиковые микропланшеты. Зараженные культуры инкубировали при 15°С.
Идентификацию выделенных изолятов SbSHV проводили реакцией нейтрализации с гипериммунной антисывороткой против герпесвирусной болезни сибирского осетра, а также методом ПЦР-РВ с помощью набора реагентов для выявления ДНК вируса SbSHVD «АмплиПрайм® Герпесвирус сибирского осетра» (Некст-Био, г. Москва) [13, 14, 15].
Для изучения оптимальных условий долгосрочного хранения герпесвируса вируссодержащую культуральную жидкость культуры SSO-2, зараженную изолятом SK/0406, после полного разрушения монослоя расфасовывали в пробирки Эппендорф с 10% фетальной телячьей сыворотки и сохраняли на трех разных температурах: +4°С; -18°С; -80°С. Через определенные интервалы времени отбирали по две пробирки, ресуспендировали их и заражали культуру SSO-2 для определения титра вируса. Предварительно определяли исходный титр вируса методом Рида и Менча [16].
Во время проведения работ соблюдали правила биологической безопасности при осуществлении работ с использованием патогенных биологических агентов [17].
Результаты исследований и их обсуждение. В коллекции накоплены бактерии: Aeromonas hydrophila, A. veronii, A. salmonicida, A. eucrenophila, Pseudomonas alcaligenes (2 штамма), Pseudomonas sp. и изоляты герпесвируса сибирского осетра (табл. 1).
Штаммы бактерий выделены от лососевых, осетровых и карповых рыб в рыбоводных хозяйствах Центрального федерального округа Российской Федерации при наличии клинических признаков и без таковых (рисунок 1).
Таблица 1 Перечень штаммов бактерий и изолятов герпесвируса в коллекции лаборатории
| № пп | Наименование штамма | Место и год выделения штамма | Объект исследования и наличие сопутствующих клинических и патологоанатомических признаков заболевания |
|---|---|---|---|
| Бактерии | |||
| 1 | Aeromonas hydrophila 89-2пэр1-21 | Московская обл., рыбоводное хозяйство, май, 2021 г. | Карп, с характерными клиническими и патологоанатомическими признаками аэромоноза, выделен из печени |
| 2 | Aeromonas veronii 89-5пчэр1-21 | Московская обл., рыбоводное хозяйство, май, 2021 г. | Белый амур, с характерными клиническими и патологоанатомическими признаками аэромоноза, выделен из почек |
| 3 | Aeromonas salmonicida 4-6кАО-24 | Тверская обл., рыбоводное хозяйство, январь 2024 г. | Форель радужная, без клинических признаков заболевания, выделен из кишечника |
| 4 | Aeromonas eucrenophila 87-2АО-24 | Тверская обл., рыбоводное хозяйство, май 2024 г. | Личинка стерляди, диагностирована бактериальная геморрагическая септицемия |
| 5 | Pseudomonas alcaligenes 11 эр1-25 | Тверская обл., индустриальное рыбоводное хозяйство, февраль 2025 г. | Личинки осетровых рыб, диагностирована бактериальная геморрагическая септицемия |
| 6 | Pseudomonas alcaligenes 211-11кЙ-24 | Республика Карелия, индустриальное рыбоводное хозяйство, октябрь 2024 г. | Форель радужная, без клинических признаков заболевания, выделен из кишечника |
| 7 | Pseudomonas sp. 23-3пчэр1-25 | Смоленская обл., индустриальное рыбоводное хозяйство, февраль 2025 г. | Форель радужная молодь, без клинических признаков заболевания, выделен из почек |
| Изоляты герпесвируса (SbSHV) | |||
| 8 | SK/0406 | Центральный ФО, 2006 г. | Молодь сибирского осетра ленской популяции, с характерными клиническими и патологоанатомическими признаками SbSHV |
| 9 | SF/1210 | Финляндия, частное рыбоводное хозяйство, 2010 г. | Молодь сибирского осетра ленской популяции, с характерными клиническими и патологоанатомическими признаками SbSHV |
| 10 | IZ/0311 | Приволжский ФО, 2011 г. | Молодь сибирского осетра, с характерными клиническими и патологоанатомическими признаками SbSHV |
| 11 | SK/1114 | Центральный ФО, 2014 г. | Молодь сибирского осетра без клинических признаков SbSHV |
| 12 | VS/0119 | Центральный ФО, 2019 г. | Годовик сибирского осетра ленской популяции, без клинических признаков SbSHV |
| 13 | RAzn/0623 | Азербайджан, частное осетровое хозяйство, 2023 г. | Молодь русского осетра, с характерными клиническими и патологоанатомическими признаками SbSHV |
Таблица 2 Результаты по оценке сохранности ростовых свойств и патогенности бактерий р. Aeromonas
| Условия хранения 1 | Рост на питательной среде (эритритагар), % проб / ДНК-азная активность, зона деполимеризации ДНК, мм | |||
|---|---|---|---|---|
| A. hydrophila | A. veronii | A. salmonicida | A. eucrenophila | |
| Срок хранения, сут. | 368 | 172 | ||
| Криоконсервация в сжиженном азоте (t= -196 °С) | 100 % – обильный рост* / 1,0 мм | 100 % – обильный - сливной рост / 3,5 мм | 100 % – обильный- сливной рост /1,0 мм | 100% – обильный - сливной рост */ 3,0 мм |
| Замораживание при ультранизкой температуре (t= -80 °С) | 100 % – обильный рост / 1,0 мм | 100 % – обильный рост/ 3,0 -3,5 мм | 100 % – обильный- сливной рост / 1,0 мм | 100% – обильный- сливной рост / 3,0-4,0 мм |
| Охлаждение (t= +4 - +8 °С) | 100 % – обильный- сливной рост / 1,5 мм | 100 % - обильный- сливной рост / 3,0-3,5 мм | 100% – обильный- сливной рост / 1,5- 2,0 мм | 100% – обильный- сливной рост / 2,0-3,0 мм |
Таблица 3 Результаты по оценке сохранности ростовых свойств и патогенности бактерий р. Pseudomonas
| Криоконсервация в сжиженном азоте (t=-196°С) | Рост на питательной среде (эритритагар), % проб | ||
|---|---|---|---|
| A. hydrophila | A. veronii | A. salmonicida | |
| Срок хранения, сут. | 40 | ||
| Криоконсервация в сжиженном азоте | 100% – обильный- сливной | 100% – обильный - сливной | 100% – обильный- сливной |
| (t=-196°С) | рост* | рост | рост |
| Замораживание при ультранизкой | 100% – обильный- сливной | 100% – обильный- сливной | 100% – обильный- сливной |
| температуре (t=-80°С) | рост | рост | рост |
| Охлаждение | 100% – обильный- сливной | 100% – обильный- сливной | 100% – обильный- сливной |
| (t=+4 – +8°С) | рост | рост | рост |

Рис. 1. Карп, с клиническими признаками бактериальной инфекции (бактериальная геморрагическая септицемия)
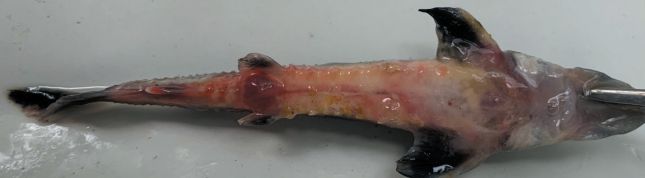
Рис. 2. Рыба с клиническими признаками герпесвирусного заболевания
Оценка жизнеспособности бактерий р. Aeromonas и их патогенности после хранения показала высокую сохранность культур (у 100 % проб регистрировали обильный и сливной рост) при всех режимах (табл. 2).
По степени сохранения патогенности (вирулентности) бактерий были получены нестабильные результаты. У бактерии А. hydrophila вирулентность (ДНК-азная активность) уменьшилась до минимальной, у A. eucrenophila – снизилась незначительно, у A. veronii и A. salmonicida – была близка к вирулентности, существующей на момент закладки штаммов на хранение. Необходимо отметить, что у A. salmonicida, хранившихся при t= +4-+8 °С, вирулентность сохранилась на более высоком уровне, чем при других режимах хранения.
В 2025 г. для пополнения коллекции патогенных бактерий были заложены три изолята полевых штаммов р. Pseudomonas, выделенных из патматериала рыб. Первую проверку сохранности ростовых свойств и патогенности изолятов бактерий р. Pseudomonas провели по истечении 40 суток хранения.
У всех штаммов в 100 % проб выявили жизнеспособные клетки и высокую сохранность ростовых свойств (обильный-сливной рост на свежем питательном агаре) (табл. 3).
Биохимические свойства бактериальных культур выросших штаммов проверяли на агаре Клиглера и среде Хью-Лейфсона, выявили отсутствие ферментации глюкозы, образования кислоты из лактозы и продуцирование сероводорода, защелачивание среды, положительную реакцию на цитохромоксидазу, положительный каталазный тест, окисление глюкозы (у Pseudomonas sp.) и инертность к глюкозе (у Pseudomonas alcaligenes) и подвижность. Выявленные свойства подтвердили принадлежность бактерий к р. Pseudomonas.
Изоляты герпесвируса сибирского осетра были выделены от сибирского и русского осетров и их гибридов с клиническими и патологоанатомическими признаками, характерными для герпесвирусной болезни (рисунок 2).
Изоляты вируса выделены из покровных тканей и внутренних органов разновозрастной молоди в чувствительных культурах клеток SSO-2 и WSS-2 во время заболевания или при мониторинговых исследованиях хозяйств. Последующая идентификация выделенных цитопатогенных агентов методами нейтрализации гипериммунной антисывороткой и в ПЦР-РВ подтвердила наличие герпесвируса сибирского осетра (табл. 4).
Таблица 4 Результаты идентификации выделенных изолятов вируса в ПЦР-РВ
| Исследуемый материал | Титр вируса в культуре клеток SSO-2, lg ТЦД50/мл | Результат ПЦР-РВ (SbSHV) HEX (значение Cq) |
|---|---|---|
| Интактная клеточная культура WSS-2 | н.о. | н.о. |
| Интактная клеточная культура SSO-2 | н.о. | н.о. |
| SbSHV SK/1114 | 6,1 | 17,35 |
| SbSHV Iz 6/0311 | 5,75 | 22,25 |
| SbSHV SF/1210 | 4,1 | 25,35 |
| SbSHV Sk/0406 | 6,1 | 17,75 |
| SbSHV VS/0119 | 5,8 | 39,18 |
| SbSHV RAzn/0623 | 4,8 | 20,30 |
Примечание: н.о. – не определено
Эффективность сохранности вируса проверяли на изоляте SbSHV Sk/0406. Результаты исследований по определению оптимальных условий долгосрочного хранения герпесвируса показали, что при +4°С вирус сохранялся лучше, чем при -18°С в течение всего периода наблюдения (3 месяца). Данный факт отличает вирус SbSHV от других вирусов рыб (например, рабдови-русы инфекционного гемопоэтического некроза, вирусной геморрагической септицемии, весенней виремии карпа и др.), которые хорошо сохраняются продолжительное время при -18°С.
При хранении в температуре -80°С титр вируса не снижался, при +4°С за 3 месяца инфекционная активность снизилась на 3 lg ТЦД50/мл, а при хранении в -18 °С – на 4,17 lg ТЦД50/мл при титровании в культуре клеток SSO-2 (рисунок 3).
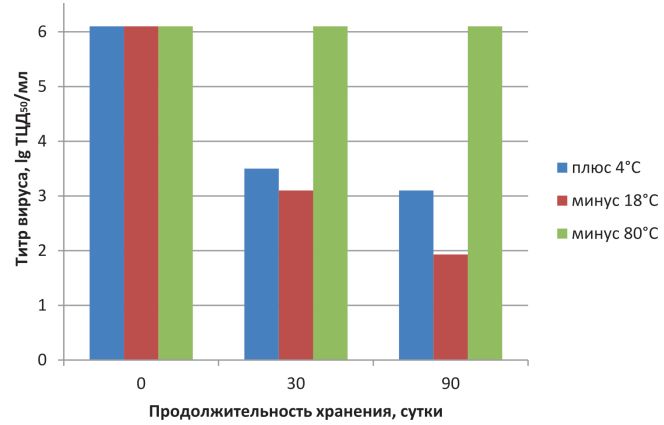
Рис. 3. Сохранность герпесвируса сибирского осетра при разных температурах
Заключение. Формирующаяся коллекция патогенов-возбудителей заболеваний рыб в лаборатории ихтиопатологии Филиала по пресноводному рыбному хозяйству ФГБНУ «ВНИРО» («ВНИИПРХ») включает штаммы бактерий р.р. Aeromonas и Pseudomonas, изоляты гепресвируса сибирского осетра (SbSHV). Аэромонады и псевдомонады относятся к эпизоотически значимым возбудителям бактериальных заболеваний, в некоторых случаях провоцирующих эпизоотии с высокими потерями гидробионтов. Штаммы бактерий, находящихся в коллекции лаборатории, выделены от лососевых, осетровых и карповых рыб в рыбоводных хозяйствах различного типа Центрального федерального округа Российской Федерации. В настоящее время в коллекции лаборатории находится 7 штаммов бактерий: Aeromonas hydrophila, A. veronii, A. salmonicida, A. eucrenophila, Pseudomonas sp. и 2 штамма Pseudomonas alcaligenes. У бактерий в течение года хранения выявили высокую сохранность штаммов (у 100% проб обильный и сливной рост) при всех используемых режимах: криоконсервация в сжиженном азоте (t=-196°С), замораживание при ультранизкой температуре (t=-80°С) и охлаждение (t=+4-+8°С). Патогенность (вирулентность) штаммов имела тенденцию к снижению, наиболее значимо ДНК-азная активность снизилась у бактерии А. hydrophila. Изоляты SbSHV, находящиеся в коллекции, выделены в разных регионах Российской Федерации и ближнего зарубежья от разновозрастной молоди сибирского, русского осетров и их гибридов. В коллекции заложено 6 изолятов герпесвируса, перед размещением на хранение у каждого изолята проверяли инфекционную активность, все варианты были с достаточно высоким титром от 4,1 до 6,1 lg ТЦД50/мл. По истечению 3 месяцев хранения герпесвируса сибирского осетра оптимальной являлась температура -80°С в условиях низкотемпературного морозильника. Отраслевая исследовательская коллекция патогенов в лаборатории ихтиопатологии будет пополняться другими высокопатогенными изолятами бактерий и вирусов, эпизоотически значимыми для рыб.
Список литературы:
1. Carvalho M. J., Martinez-Murcia A., Esteves A. C. et al. Phylogenetic diversity, antibiotic resistance and virulence traits of Aeromonas spp. from untreated waters for human consumption. International Journal of Food Microbiology. 2012; 159 (3): 230-239.
2. Минаева А. Н., Ломакин А. А., Васильев Д. А. [и др.]. Общая характеристика бактерий вида Aeromonas veronii. Евразийский Союз Ученых. 2021; 2 (83): 7-9.
3. Pseudomonas (псевдомонады, род бактерий) https://gastroscan.ru/ handbook/118/4160.
4. Хоулт Дж, Крига Н., Снита П. [и др.]. Определитель бактерий Берджи. Т. 1. Мир. 1997: 432 с.
5. Iglewski B. H. Pseudomonas. Medical Microbiology. 4th ed. Galveston: University of Texas Medical Branch at Galveston. 1996. https://www.ncbi.nlm.nih.gov/books/ NBK8326/.
6. Щелкунов И. С., Щелкунова Т. И., Щелкунов А. И. [и др.]. Герпесвирусная болезнь у осетровых рыб в России. Российский ветеринарный журнал. Сельскохозяйственные 36 животные. 2007; (1): 10-12.
7. Doszpoly A., Shchelkunov I. Partial genome analysis of siberian sturgeon alloherpesvirus suggests its close relation to ACIHV-2-short communication. Acta Veterinaria Hungarica. 2010; 58 (2): 269-274.
8. Davison A., Eberle R., Ehlers B. et al. The order Herpesvirales. Archives of Virology. 2009; 154 (1): 171-177.
9. Shchelkunov A. I., Shchelkunov I. S., Shchelkunova T. I. et al. Isolation of a herpesvirus causing acute disease in juvenile Siberian sturgeon. Khaled bin Sultan Living Oceans Foundation. 2011: 345-346.
10. Методические указания по определению патогенности аэромонад по степени ДНКазной активности. Сборник инструкций по борьбе с болезнями рыб. Ч. 1. Отдел маркетинга АМБ-агро. 1998: 150-151.
11. Методические указания по идентификации вирусов и лабораторной диагностике вирусных болезней рыб. Сборник инструкций по борьбе с болезнями рыб. Ч. 1. Отдел маркетинга АМБ-агро. 1998: 60-75.
12. Manual of Diagnostic Tests for Aquatic Animals. 8th ed. OIE. 2017.
13. Щелкунов И. С., Щелкунов А. И., Щелкунова Т. И. [и др.]. Методические рекомендации по диагностике герпесвирусной болезни сибирского осетра. 2009: 10 с.
14. Барышникова Е. И., Сенина М. Е., Щелкунова Ю. П. [и др.]. Разработка тест-системы для выявления ДНК герпесвируса сибирского осетра методом ПЦР в режиме реального времени. Ветеринария. 2023; (2): 25-29.
15. Щелкунова Ю. П., Барышникова Е. И., Сенина М. Е. [и др.]. Чувствительность лабораторных методов диагностики герпесвирусной болезни у гибрида осетровых рыб. Ветеринария. 2023; (3): 31-37.
16. Lei C., Yang J., Hu J. et al. On the Calculation of TCID50 for Quantitation of Virus Infectivity. Virologica Sinica. 2021; 36: 141-144.
17. Санитарные правила и нормы СанПиН 3.3686-21 «Санитарно-эпидемиологические требования по профилактике инфекционных болезней» (утв. постановлением Роспотребнадзора от 28 января 2021 г. № 4, ред. 25 мая 2022 г.).
Сведения об авторах:
Токарева Светлана Борисовна, главный специалист лаборатории ихтиопатологии Филиала по пресноводному рыбному хозяйству ФГБНУ «Всероссийский научно-исследовательский институт рыбного хозяйства и океанографии»; 141821, Московская область, Дмитровский городской округ, пос. Рыбное, 40 А; тел.: 8-495-1086856 (добавочный – 132); e-mail: tokareva@vniiprh.vniro.ru.
Щелкунова Юлия Петровна, кандидат биологических наук, заместитель заведующего лаборатории ихтиопатологии Филиала по пресноводному рыбному хозяйству ФГБ-НУ «Всероссийский научно-исследовательский институт рыбного хозяйства и океанографии»; 141821, Московская область, Дмитровский городской округ, пос. Рыбное, 40 А; тел.: 8-495-1086856 (добавочный – 118); e-mail: schelkunova@vniiprh.vniro.ru.
Ответственный за переписку с редакцией: Романова Наталья Николаевна, кандидат биологических наук, доцент, заведующий лабораторией ихтиопатологии Филиала по пресноводному рыбному хозяйству ФГБНУ «Всероссийский научно-исследовательский институт рыбного хозяйства и океанографии»; доцент кафедры «Аквакультура и экология» Дмитровского рыбохозяйственного технологического института (филиала) Астраханского государственного технического университета; доцент кафедры кормления и кормопроизводства Московской государственной академии ветеринарной медицины и биотехнологии – МВА имени К.И. Скрябина; 141821, Московская область, Дмитровский городской округ, пос. Рыбное, 40 А; тел.: 8-495-1086856 (добавочный – 132); e-mail: romanova@vniiprh.vniro.ru.
Заявленный вклад авторов: рукопись была написана благодаря вкладу всех авторов. Все авторы одобрили окончательную версию рукописи.
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
http://www.vetkuban.com/num1_202609.html