|
||||

Гематологическая и патоморфологическая картина при микотоксикозе у поросятУДК 619; 576; 579.62 Оригинальное эмпирическое исследование Миронова А. А. Северо-Кавказский зональный научноисследовательский ветеринарный институт – филиал Федерального Аннотация. Микотоксины – опасные для здоровья животных и человека вещества, обладающие ядовитыми свойствами. Т-2 токсин – часто встречающийся микотоксин, продуцируемых грибами рода Fusarium. Охратоксины продуцируются штаммами грибов родов Penicillium и Aspergillus. Загрязнение кормов происходит, как правило, не одним, а несколькими микотоксинами одновременно, способными усиливать и пролонгировать действие друг друга на живой организм. Свиньи наиболее чувствительны к Т-2 токсину и охратоксину А. Целью было изучить влияние Т-2 токсина и сочетания Т-2 токсина и охратоксина на гематологическую и патоморфологическую картину у поросят. Материалы и методы исследований. Был проведен опыт по установлению токсичности Т-2 токсина и охратоксина на поросятах, которым с месячного возраста давали корм с микотоксинами. В возрасте 2 и 3 месяца животных исследовали по показателям: масса тела, среднесуточный прирост; в крови определяли: содержание лейкоцитов, эритроцитов, гемоглобина, гематокрит, СОЭ на ветеринарном гематологическом анализаторе Mindray BC-2800Vet. Трупы павших и вынужденно убитых животных исследовали согласно принятым в патологической анатомии методам вскрытия, описания органов и патологических процессов. Результаты исследований и их обсуждение. В результате исследований было установлено, что сочетанное влияние Т-2 токсина и охратоксина оказало более выраженное токсическое действие на организм поросят: в двухмесячном и трехмесячном возрасте были достоверно ниже: масса тела, среднесуточный прирост, число лейкоцитов (лейкопения), эритроцитов (эритропения), гематокрит, уровень гемоглобина (гемоглобинемия); СОЭ – достоверно выше; к трехмесячному возрасту 6 поросят пали, 4 были вынужденно убиты; при вскрытии установлены патологоанатомические диагнозы: эксикоз, истощение, застойная гиперемия и отек легких, альтеративный миокардит, острый катарально-фибринозный энтероколит, острый катаральный энтероколит, застойная гиперемия, отек серозных оболочек и брыжейки кишечника, застойная гиперемия и отек стенок тонкого и толстого отделов кишечника, острый серозный лимфаденит мезентериальных лимфоузлов, токсическая дистрофия печени, застойная гиперемия и отек селезенки, зернистая дистрофия почек, застойная гиперемия и отёк головного мозга, застойная гиперемия и отек подкожной клетчатки, геморрагический диатез, на основании чего был поставлен нозологический диагноз – микотоксикоз. Заключение. У поросят, получавших корм с Т-2 токсином, гематокрит снижался по сравнению с контролем, СОЭ увеличивалась, среднесуточные приросты снижались, регистрировались лейкопения и эритропения. У поросят, получавших корм с Т-2 токсином и охратоксином, снижалась масса тела в сравнении с контролем, регистрировались лейкопения, эритропения и гемоглобинемия, СОЭ увеличивалась. Патологоанатомические диагнозы были характерными для микотоксикозов. Сочетанное влияние Т-2 токсина и охратоксина оказало более выраженное токсическое действие на организм поросят. Ключевые слова: микотоксины, Т-2 токсин, охратоксин, масса тела, среднесуточный прирост, гематологические показатели, патологоанатомические диагнозы. В 80-100% сельскохозяйственной и пищевой продукции выявляются микроскопические грибы, продуцирующие микотоксины, причем, в 40-60% случаев это токсиген-ные штаммы, продуктами жизнедеятельности которых являются микотоксины – опасные для здоровья вещества, обладающие ядовитыми свойствами. Они получили свое название от греческого слова mykes – гриб и toxicon – яд [1, 2, 3]. При поедании кормов, пораженных токсигенными плесневыми грибами и их метаболитами, у животных могут возникать острые и хронические отравления [4, 5], характеризующиеся поражением печени, почек, нервной, эндокринной и репродуктивной систем, кожными патологиями и влиянием на метаболические процессы. Большие дозы микотоксина вызывают ярко-выраженные признаки; при поступлении малых доз развивается хроническое течение с незначительными клиническими проявлениями, что затрудняет диагностику микотоксикоза [6, 7]. Микотоксины через пищевую цепь могут попасть и к человеку, у которого действуют подавляюще на иммунитет и даже могут вызвать опухолевые заболевания [8, 9]. Российским Законодательством установлены предельно допустимые концентрации (ПДК) для 5 микотоксинов [10]. Так, содержание афлатоксина в кормах должно составлять не более 0,025-0,1 мг/ кг, дезоксиниваленола – не более 0,75-1,0 мг/ кг, Т-2 токсина – не более 0,1 мг/ кг, зеараленона – не более 1,0 мг/ кг, охратоксина А – не более 0,05 мг/ кг [11, 12]. Т-2 токсин наиболее часто встречающийся микотоксин, из более чем 40 трихотеценовых токсинов, продуцируемых грибами рода Fusarium. Наиболее часто причиной отравлений служит Т-2 токсин, особенно для организма кур, уток и свиней. Т-2 токсин обладает выраженным токсическим действием, ингибируя процессы инициации трансляции на этапе перед образованием комплекса между рибосомой, информационной РНК, блокирует процесс образования белка [13]. Охратоксины продуцируются штаммами грибов родов Penicillium и Aspergillus, которые любят условия высокой влажности [14]. Охратоксин А был обнаружен как естественный контами-нант на кукурузе, пшенице, овсе, ячмене, ржи и некоторых бобах (кофейные и соевые бобы, бобы какао) во многих регионах мира [15 ]. Из всех сельскохозяйственных животных свиньи наиболее чувствительны к охратоксину А. Хроническое течение охратокси-коза встречается наиболее часто в свиноводческих хозяйствах без выраженных клинических признаков. Однако отмечают угнетение, полиурию, снижаются темпы прироста [16, 17]. Проблема осложняется тем, что загрязнение кормов происходит, как правило, не одним, а несколькими микотоксинами одновременно. При этом, если даже степень токсичности отдельных микотоксинов не превышает МДУ, то они способны усиливать и пролонгировать действие друг друга на живой организм, вызывая иммуносупрессию, задержку роста, развития и продуктивности, снижая устойчивость к инфекционным заболеваниям [18, 19]. Материалы и методы исследований. Для установления токсичности продуцируемых выделенными микромицетами Т-2 токсина и охратоксина провели опыт на поросятах, которым с месячного возраста давали корм с микотоксинами: поросята первой опытной группы получали с Т-2 токсином из расчета 0,1-0,2 мг/ кг; поросята второй группы – с Т-2 токсином из расчета 0,1-0,2 мг/ кг и охратоксином из расчета 0,02-0,1 мг/ кг; первая группа (контроль) получала корм с Т-2 токсином и охратоксином ниже ПДК. В возрасте 2 и 3 месяца животных исследовали по показателям: масса тела, среднесуточный прирост; в крови определяли: содержание лейкоцитов, эритроцитов, гемоглобина, гематокрит, СОЭ на ветеринарном гематологическом анализаторе Mindray BC-2800Vet. Трупы павших и вынужденно убитых животных исследовали согласно принятым в патологической анатомии методам вскрытия, описания органов и патологических процессов. Цель: изучить влияние Т-2 токсина и сочетания Т-2 токсина и охратоксина на гематологическую и патоморфологическую картину у поросят, для достижения которой были поставлены к решению следующие задачи: 1) определить массу тела, среднесуточный прирост; 2) определить гематологические показатели у поросят в возрасте 2-3 мес.; 3) исследовать патоморфологиче-ские признаки у павших и вынужденно убитых животных. Результаты исследований и их обсуждение. Полученные в ходе проведения исследований результаты отражены в таблице и рисунках 1, 2, 3, 4, 5 и 6. Таблица 1 Влияние микотоксинов на массу тела, показатели прироста и картину крови подопытных поросят
Примечание: *p<0,05; **p<0,01; ***p<0,001 по сравнению с контрольной группой В двухмесячном возрасте поросята контрольной группы (Т-2 токсин и охратоксин ниже ПДК) имели живую массу в среднем 18,3 кг, что было больше на 1,1 кг по сравнению с молодняком первой опытной группы (разница недостоверна). Животные второй группы уступали им 2,4 кг (p<0,05). Поросята первой и второй опытных групп характеризовались меньшими среднесуточными приростами живой массы на 5,3 (разница недостоверна) – 15,4% (p<0,05), соответственно. У двухмесячных поросят первой опытной группы средний уровень лейкоцитов был в 1,2 раза ниже, чем в контроле (p<0,05); у животных второй группы он был в 1,9 раза ниже в сравнении с контролем (p<0,001) – лейкопения. У животных первой опытной группы среднее число эритроцитов и уровень гемоглобина были ниже таковых в сравнении с контрольной группой на 21,2% и 14,5% (p<0,05). У поросят второй опытной группы число эритроцитов было меньше в сравнении с контролем на 43,9% (p<0,01); уровень гемоглобина был ниже в сравнении с контролем на 19,2% (p<0,05). Средний показатель гематокрита у животных в контрольной группе был выше в сравнении с животными первой опытной группы на 23,3% (p<0,05) и второй опытной группы – на 37,2% (p<0,01). СОЭ у поросят первой опытной группы была выше в сравнении с контролем в 1,7 раза (p<0,001), у поросят второй опытной группы – в 4,6 раза (p<0,001). В трехмесячном возрасте поросята контрольной группы имели живую массу в среднем 30,9 кг, что было больше на 3,7 кг по сравнению с молодняком первой группы (разница недостоверна) и на 6,8 кг больше в сравнении с поросятами второй группы (р<0,05). У поросят первой и второй опытных групп также были меньшие среднесуточные приросты живой массы на 21,4% (р<0,05) – 35,3% (р<0,01), соответственно. У трехмесячных поросят первой опытной группы средний уровень лейкоцитов был в 1,4 раза ниже, чем в контроле (p<0,01); у животных второй группы он был в 1,8 раза ниже в сравнении с контролем (p<0,001) – лейкопения. У животных первой опытной группы среднее число эритроцитов и уровень гемоглобина были ниже таковых в сравнении с контрольной группой на 37,7% (p<0,01) и 12,0% (разница недостоверна) соответственно. У поросят второй опытной группы среднее число эритроцитов было меньше в сравнении с контролем на 43,9% (p<0,01); уровень гемоглобина был ниже на 22,1% (p<0,05). Средний показатель гематокрита у животных в контрольной группе был выше в сравнении с животными первой опытной группы на 23,3% (p<0,05) и второй опытной группы – на 37,2% (p<0,01). СОЭ у поросят первой опытной группы была выше в сравнении с контролем в 1,7 раза (p<0,001), у поросят второй опытной группы – в 4,6 раза (p<0,001). Таким образом, у поросят, получавших корм с Т-2 токсином, в двухмесячном возрасте гематокрит был достоверно ниже в сравнении с контролем, СОЭ – достоверно выше; в трехмесячном возрасте – достоверно ниже среднесуточные приросты, число лейкоцитов (лейкопения) и эритроцитов (эритропения). У поросят, получавших корм с Т-2 токсином и охратоксином, в двухмесячном и трехмесячном возрасте были достоверно ниже масса тела, среднесуточный прирост, число лейкоцитов (лейкопения), эритроцитов (эритропения), гематокрит, уровень гемоглобина (гемогло-бинемия), СОЭ была достоверно выше. В возрасте три месяца 6 поросят из третьей опытной группы, получавших корм с Т-2 токсином и охратоксином, пали, 4 были вынужденно убиты. При осмотре установлено, что окоченение выражено в разной степени у всех трупов поросят, щетина тусклая, взъерошенная. У всех павших животных щетинки в области ануса склеены жидкими каловыми массами, у всех присутствуют признаки обезвоживания и истощения. Лёгкие у всех трупов и вынужденно убитых животных темно-красного цвета с синюшным оттенком, с поверхности разреза стекает красного цвета содержимое водянистой консистенции; вырезанные кусочки в воде находились в полупогруженном состоянии (застойная гиперемия и отек) (рисунок 1).
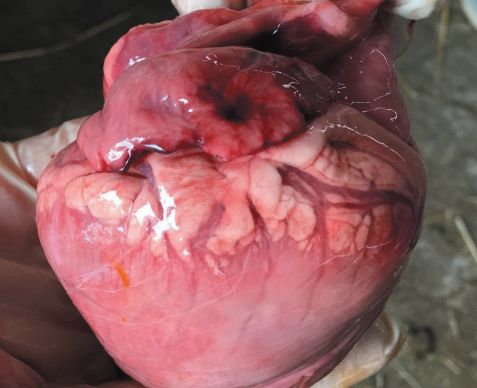
Рис. 1. Застойная гиперемия и отек лёгких Сердечная мышца у всех павших и вынужденно убитых животных дряблая, неравномерно окрашена в серо-белый цвет (зернистая дистрофия миокарда). У всех павших и вынужденно убитых животных отдельные участки сердечной мышцы имеют вид варёного мяса (ценкеровский некроз). У всех вскрытых животных сосуды миокарда расширены, переполнены кровью, сердечная мышца местами темно-красного с синюшным оттенком цвета, сочная на разрезе, темно-красного цвета (застойная гиперемия). У всех трупов и вынужденно убитых животных сердце округлой формы, полости его переполнены тёмно-красной слабо свернувшейся кровью, соотношение толщины стенок левого и правого желудочков 1:5 – 1:10 (атрофия миокарда правого желудочка). Согласно совокупности отдельных патологоанатомических диагнозов у всех вскрытых животных альтеративный миокардит (рисунок 2). У 80,0% павших животных зарегистрирован острый катарально-фибринозный энтероколит, при котором слизистая оболочка набухшая, утолщена, сильно гиперемирована, отечна, покрыта местами творожистыми трудно снимаемыми наложениями; в промежутках между ними она сильно гиперемирована, с кровоизлияниями, обильно покрыта бесцветной слизью. Острый катаральный энтероколит, при котором слизистая оболочка кишечника гиперемирована, с кровоизлияниями, набухшая, на разрезе красного цвета, утолщена в 2-3 раза, обильно покрыта бесцветной слизью, установлен у 20,0% павших животных и у всех – вынужденно убитых. Сосуды брыжейки и серозных оболочек тонкого и толстого отделов кишечника у всех вскрытых трупов и вынужденно убитых животных расширены, переполнены кровью (застойная гиперемия), брыжейка и сальник утолщены, тестообразной консистенции, серозные оболочки набухшие, покрасневшие, блестящие (отек) (рисунок 3).
Рис. 2. Острый альтеративный миокардит (гиперемия, кровоизлияния, дистрофия, некроз)
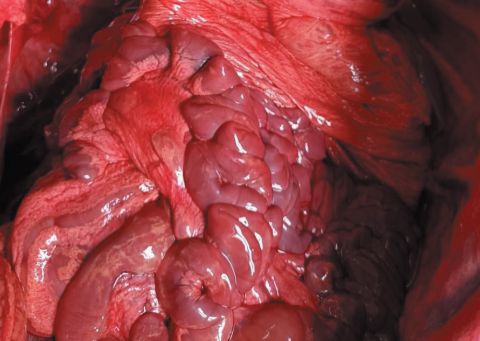
Рис. 3. Застойная гиперемия, отек брыжейки, сальника, серозных оболочек кишечника Мезентериальные лимфатические узлы у всех вскрытых трупов увеличены в 2-3 раза, упругой консистенции, сочные на разрезе, серо-красного цвета с множеством точечных кровоизлияний, поверхность разреза выбухает (острый серозный лимфаденит) (рисунок 4).
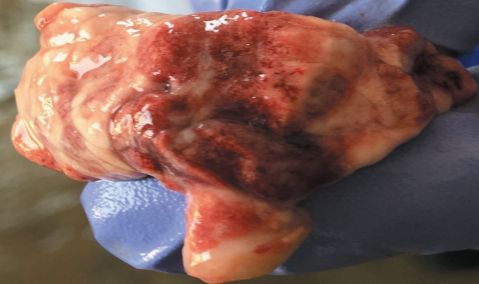
Рис. 4. Острый серозный лимфаденит (отек, кровоизлияния) мезентериального лимфоузла Селезёнка у всех трупов и вынужденно убитых животных увеличена в 1,5-2 раза с притуплёнными краями, красно-коричневого цвета, плотновато-упругая, но после надавливания пальцем остается медленно восстанавливающаяся ямка, сочная на разрезе, с умеренным соскобом (застойная гиперемия и отек). Печень у всех животных увеличена, с притуплёнными краями, неравномерно пестро окрашена: небольшое количество участков тёмно-красного цвета с синюшным оттенком (застойная гиперемия), серо-белые нечётко ограниченные полосчатые или пятнистые участки, уходящие вглубь на всю толщу органа (зернистая дистрофия). У всех вскрытых трупов павших и у вынужденно убитых животных имеется много обширных, разлитых, нечётко ограниченных, охряно-желтого цвета, неправильной формы, дряблой, рвущейся консистенции участков, оставляющих при разрезании на ноже жирный налёт (жировая дистрофия). У всех трупов и вынужденно убитых поросят находили в печени мелкие, диаметром 1-2 мм серо-белые, чётко ограниченные, бесструктурные участки (милиарные ареактивные сухие некрозы), точечные диаметром 1-2 мм, четко ограниченные, множественные, темно-красные участки, беспорядочно расположенные по всей поверхности и в глубине органа (кровоизлияния) (рисунок 5).
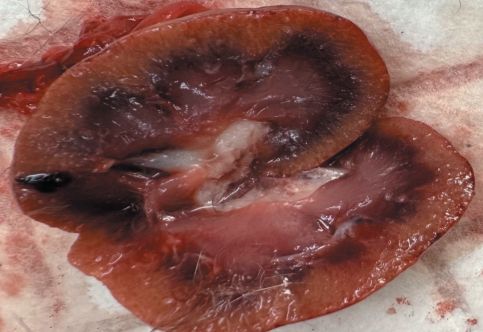
Рис. 5. Токсическая дистрофия печени Почки у всех павших животных слегка увеличены, неравномерного серо-красного цвета с нечётко ограниченными полосчатыми участками серо-белого цвета; на разрезе: поверхность разреза сочная, мутная, граница коркового и мозгового слоев сглажена (отек, зернистая дистрофия) (рисунок 6).
Рис. 6. Сглаженность коркового и мозгового слоев, отек, зернистая дистрофия почки на разрезе У всех вскрытых животных вещество головного мозга серо-розового цвета, набухшее, сочное на разрезе, содержащее в полостях боковых желудочков 2-4 мл прозрачной бесцветной жидкости (застойная гиперемия и отёк). При патологоанатомическом вскрытии были установлены следующие диагнозы: эксикоз; истощение; застойная гиперемия и отек легких; альтеративный миокардит; острый катарально-фибринозный энтероколит; острый катаральный энтероколит; застойная гиперемия, отек серозных оболочек и брыжейки кишечника; застойная гиперемия и отек стенок тонкого и толстого отделов кишечника; острый серозный лимфаденит мезентериальных лимфоузлов; токсическая дистрофия печени (зернистая и жировая дистрофия, некрозы, кровоизлияния, застойная гиперемия); застойная гиперемия и отек селезенки; зернистая дистрофия почек; застойная гиперемия и отёк головного мозга; застойная гиперемия и отек подкожной клетчатки; геморрагический диатез (кровоизлияния в подкожной и межмышечной клетчатке, на серозных и слизистых оболочках, во внутренних органах). Идентичность картины патологоанатомического вскрытия у всех трупов и совокупность патологоанатомических диагнозов позволили сделать следующее заключение: причина смерти – паралич центра дыхания в результате интоксикации микотоксинами (Т-2 токсин, охратоксин), на основании чего был поставлен нозологический диагноз – микотоксикоз. У поросят, получавших корм с Т-2 токсином, в двухмесячном возрасте гематокрит был достоверно ниже в сравнении с контролем, СОЭ – достоверно выше; в трехмесячном возрасте – достоверно ниже среднесуточные приросты, число лейкоцитов (лейкопения) и эритроцитов (эритропения). У поросят, получавших корм с Т-2 токсином и охратоксином, в двухмесячном и трехмесячном возрасте были достоверно ниже масса тела, среднесуточный прирост, число лейкоцитов (лейкопения), эритроцитов (эритропения), гематокрит, уровень гемоглобина (гемоглобинемия), СОЭ – достоверно выше. Патологоанатомические диагнозы: эксикоз, истощение, застойная гиперемия и отек легких, альтеративный миокардит, острый катарально-фибринозный энтероколит, острый катаральный энтероколит, застойная гиперемия, отек серозных оболочек и брыжейки кишечника, застойная гиперемия и отек стенок тонкого и толстого отделов кишечника, острый серозный лимфаденит мезентериальных лимфоузлов, токсическая дистрофия печени, застойная гиперемия и отек селезенки, зернистая дистрофия почек, застойная гиперемия и отёк головного мозга, застойная гиперемия и отек подкожной клетчатки, геморрагический диатез. Сочетанное влияние Т-2 токсина и охратоксина оказало более выраженное токсическое действие на организм поросят. Список литературы: 1. Антипов В. А., Васильев В. Ф. Микотоксикозы – важная проблема животноводства. Ветеринария. 2007; (11): 7-9. 2. Донник И. М., Безбородова Н. А. Мониторинговые исследования микотоксинов в кормах и комбикормовом сырье в Уральском регионе. Аграрный вестник Урала. 2009; (8 (62)): 87-89. 3. Иванов А. В., Фисинин В. И., Тремасов М. Я., Папуниди К. Х. Микотоксины (в пищевой цепи). Росинформагротех. 2012: 140 с. 4. Прудников В. С., Прудников А. В. Микотоксикозы животных (патоморфология, диагностика и профилактика). Ученые записки УО Витебская государственная академия ветеринарной медицины. 2011; 47 (1): 111-114. 5. Cimbalo A., Alonso-Garrido M., Font G., Manyes L. Toxity of mycotoxins in vivo on vertebrate organisms: a review. Food and Chemical Toxicology. 2020; 137: 111161. 6. Конноли Э., О’Сулливан Д. Серия семинаров по микотоксинам: Почему сейчас? Значения для Европы и Европейского союза. Европейский семинар по микотоксинам. Оценка воздействия микотоксинов в Европе. 2005: 2-26. 7. Ле Бра Э. Микотоксикозы. Профилактика и лечение. Комбикорма. 2008; (3): 93-94. 8. Чулков А. К., Тремасов М. Я., Иванов А. В. О профилактике микотоксикозов животных. Ветеринария. 2007; (12): 8-10. 9. Gutzwiller A., Czegledi L., Stoll P., Bruckner L. Efficacite d’adsorbants contre les mycotoxines de Fusarium chez le porc. Revue Suisse d’Agriculture. 2005; 37 (3): 121-124. 10. ГОСТ 34140-2017. Продукты пищевые, корма, продовольственное сырье. Метод определения микотоксинов с помощью высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием. Стандартинформ; 2017: 19 c. 11. Фисинин В. И., Сурай П. Микотоксины и антиоксиданты: непримиримая борьба. Т-2 токсин – метаболизм и токсичность. Ветеринарная медицина. 2012; (3): 38-41. 12. Фисинин В. И., Сурай П. Микотоксины и антиоксиданты: непримиримая борьба. Охратоксин А. Комбикорма. 2012; (3): 55-56. 13. Иванов А. В., Тремасов М. Я., Папуниди К. Х. Микотоксикозы животных (этиология, лечение, профилактика). Колос. 2008: 177 с. 14. Монастырский О. А., Искандеров М. Я. Микотоксины – глобальная проблема безопасности продуктов. Агрохимия. 2016; (6): 67-71. 15. Bose S., Sinha S. Modulation of ochratoxin-produced genotoxicity in mice by vitamin C. Food Chemical and Toxicology. 1994; 32 (6): 533-537. 16. Fuchs S., Sontag G., Stidl R. et al. Detoxification of patulin and ochratoxin A, two abundant mycotoxins, by lactic acid bacteria. Food and Chemical Toxicology. 2008; 46 (4): 1398-1407. 17. Muller G., Kielstein P., Rosner H. et al. Studies of the influence of ochratoxin A on immune and defence reactions in weaners. Mycoses. 1999; 42 (7/8): 495-505. 18. Тремасов М. Я. Профилактика микотоксикозов животных в России. Ветеринария. 2002; (9): 3-8. 19. Зазимко М. А., Забашта Н. Н., Мирошниченко П. В., Данильченко О. Б., Ли-совицкая Е. П. Видовой состав микроскопических грибов в кормах, используемых в Краснодарском крае. Кормопроизводство. 2022; (5): 36-38. Сведения об авторах: Амерханов Харон Адиевич, академик РАН, доктор сельскохозяйственных наук, профессор, профессор ФГБОУ ВО РГАУ-МСХА имени К.А. Тимирязева; 127434, г. Москва, ул. Тимирязевская, 49; e-mail: h.amerhanov@yandex.ru. Миронова Ольга Анатольевна, кандидат биологических наук, доцент, заведующий базовой кафедрой биологии и безопасности экосистем института экологии ФГАОУ ВО «Российский университет дружбы народов имени Патриса Лумумбы»; ФГБУ «Всероссийский центр карантина растений»; 117198, г. Москва, ул. Миклухо-Маклая, 6. Василенко Вячеслав Николаевич, доктор сельскохозяйственных наук, член-корреспондент РАН, главный научный сотрудник Северо-Кавказского зонального научно-исследовательского ветеринарного института – филиала ФГБНУ «Федеральный Ростовский аграрный научный центр»; 346421, Ростовская область, г. Новочеркасск, Ростовское шоссе, 0. Миронова Людмила Павловна, доктор ветеринарных наук, профессор кафедры терапии и пропедевтики ФГБОУ ВО «Донской государственный аграрный университет»; главный научный сотрудник Северо-Кавказского зонального научно-исследовательского ветеринарного института – филиала ФГБНУ «Федеральный Ростовский аграрный научный центр»; 346493, Ростовская область, Октябрьский район, поселок Персиановский, ул. Кривошлыкова, 24; e-mail: mironova_lp@mail.ru. Ответственный за переписку с редакцией: Миронова Анна Анатольевна, доктор ветеринарных наук, главный научный сотрудник творческого коллектива по изучению инвазионных заболеваний животных Северо-Кавказского зонального научно-исследовательского ветеринарного института – филиал ФГБНУ «Федеральный Ростовский аграрный научный центр»; 346421, Ростовская область, г. Новочеркасск, Ростовское шоссе, 0; тел.: 8-903-4718275; e-mail: aa_mironova@mail.ru. Заявленный вклад авторов: рукопись была написана благодаря вкладу всех авторов. Все авторы одобрили окончательную версию рукописи. Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2011 © Ветеринария Кубани | Разработка сайта - Интернет-Имидж | |
|---|---|---|