|
||||

Разработка высокочувствительной пцр тест-системы для детекции вируса лейкоза крупного рогатого скотаУДК 619:636.2:616.98:578.828.11 Оригинальное эмпирическое исследование Петропавловский М. В., Донник И. М., Исаева А. Г., Мартынов Н. А. Федеральное государственное бюджетное научное учреждение «Уральский федеральный аграрный научно-исследовательский центр Уральского отделения Российской академии наук», Свердловская область, г. Екатеринбург Кривоногова А. С. Федеральное государственное бюджетное образовательное учреждение высшего образования «Уральский государственный аграрный Университет», Свердловская область, г. Екатеринбург Черных О. Ю. Федеральное государственное бюджетное образовательное учреждение высшего образования «Кубанский государственный аграрный университет имени И. Т. Трубилина», г. Краснодар Аннотация. Цель исследования: разработка высокочувствительной тест-системы на основе полимеразной цепной реакции в реальном времени (ПЦР-РВ) для детекции провирусной ДНК вируса лейкоза крупного рогатого скота (ВЛКРС). Материалы и методы исследований. С использованием биоинформатических методов (MEGA, UGENE, Primer3) на основе анализа 200 полногеномных последовательностей ВЛКРС были подобраны специфичные праймеры и гидролизный зонд, нацеленные на консервативный регион LTR-области провируса. Работоспособность системы проверялась на ДНК инфицированной клеточной линии FLK. ПЦР-РВ проводили с градиентом температур отжига (56-64°C). Специфичность амплификации контролировали методом электрофореза в агарозном геле. Результаты исследований и их обсуждение. Разработан набор олигонуклеотидов (прямой и обратный праймеры, зонд), обеспечивающий амплификацию специфичного фрагмента длиной 198 п.н. В ходе ПЦР-РВ получены стабильные кривые амплификации во всем диапазоне температур отжига. Электрофоретический анализ подтвердил отсутствие неспецифических продуктов и праймер-димеров. Заключение. Разработана высокоспецифичная ПЦР-система для прямого выявления провирусной ДНК ВЛКРС. Метод является перспективным инструментом для ранней диагностики инфекции, особенно в случаях низкой провирусной нагрузки, наличия материнских антител у телят и иммунотолерантности животных, когда серологические методы малоинформативны. Для полной валидации системы требуются дальнейшие исследования по оценке аналитической и диагностической чувствительности, специфичности и испытаниям на клинических образцах. Ключевые слова: вирус лейкоза крупного рогатого скота, провирусная ДНК, ПЦР в реальном времени, LTR-область, лабораторная диагностика, детекция вируса. Этиологическим агентом энзоотического лейкоза крупного рогатого скота является вирус лейкоза крупного рогатого скота (далее, ВЛКРС), относящийся к роду Deltaretrovirus семейства Retroviridae [1, 2, 3, 4, 5]. Несмотря на успешную элиминацию инфекции в большинстве европейских стран, в ряде других регионов мира лейкоз остается наиболее распространённым инфекционным заболеванием крупного рогатого скота. Согласно литературным данным, напряженная эпизоотическая ситуация, сопряженная с высоким уровнем инфицированности поголовья лейкозом зарегистрирована в Аргентине, Бразилии, Канаде, Японии, США, а также и в Российской Федерации [6, 7, 8, 9, 10, 11, 12]. Иммуносупрессия, развивающаяся у инфицированных животных даже на субклинической стадии, приводит к снижению общей продуктивности [13]. Таким образом, ВЛКРС оказывает значительное негативное влияние на здоровье и продуктивность поголовья, нанося существенный экономический ущерб за счёт прямых и косвенных потерь. К прямым убыткам относят снижение молочной продуктивности, ухудшение репродуктивных показателей, повышенную восприимчивость к вторичным инфекциям и преждевременную выбраковку животных. Косвенные потери связаны с ограничениями при наложении карантина, в том числе при торговле скотом, а также необходимостью выполнения дополнительных диагностических и лечебно-профилактических и организационно-хозяйственных мероприятий согласно действующим ветеринарным правилам [14, 15, 16, 17, 18]. В настоящее время, при отсутствии специфической терапии, основой (или единственной эффективной стратегией) противоэпизоотических мероприятий является своевременная диагностика с последующей изоляцией и выбраковкой инфицированных животных. Для диагностики энзоотического лейкоза применяют методы, относящиеся к двум основным категориям. Первую составляют серологические тесты, направленные на выявление специфических антител к вирусным белкам в сыворотке крови. Основными антигенными мишенями являются капсидный белок p24 (кодируемый геном gag) и поверхностный гликопротеин gp51 (кодируемый геном env). К наиболее эффективным серологическим методам относятся реакция иммунодиффузии (РИД), иммуноферментный анализ (ИФА), причём ИФА в настоящее время является основным рекомендуемым ВОЗЖ (Всемирная организация по охране здоровья животных) методом для массового скрининга во многих странах [19, 20, 21, 22]. Вторую категорию составляют молекулярно-генетические методы, направленные на прямую детекцию провирусной ДНК ВЛКРС, интегрированной в геном клеток хозяина. Несмотря на преимущества серологических методов, существуют диагностические сценарии, требующие прямого выявления возбудителя. К ним относятся: диагностика телят с колостральными (материнскими) антителами, выявление животных в ранний период острой инфекции до сероконверсии, а также тестирование животных с иммунотолерантностью, не вырабатывающих специфический гуморальный ответ. В этих случаях методы амплификации нуклеиновых кислот, в частности полимеразная цепная реакция в реальном времени (ПЦР-РВ) [23], позволяют с высокой чувствительностью и специфичностью выявлять провирусную ДНК даже на фоне низкой вирусной нагрузки. Однако, как показывают данные, существующие коммерческие ПЦР-тест-системы могут демонстрировать недостаточную аналитическую чувствительность, приводящую к ложноотрицательным результатам, уровень которых в отдельных исследованиях достигает 11,5%, что подчеркивает необходимость в разработке и валидации более эффективных диагностических тест-систем ПЦР. Таким образом, целью данного исследования является разработка высокочувствительной тест-системы на основе ПЦР в реальном времени для прямого выявления провирусной ДНК ВЛКРС. Материалы и методы исследований. Работа была выполнена на базе Уральского НИВИ – структурного подразделения УрФАНИЦ УрО РАН Отдела мониторинга и прогнозирования инфекционных заболеваний лаборатории лейкоза. Подбор олигонуклеотидов. Консенсусные последовательности генов провируса ВЛКРС для подбора праймеров были получены на основе анализа 200 полногеномных последовательностей возбудителя из базы данных NCBI Virus [26]. Множественное выравнивание выполняли в программе MEGA [24], а построение консенсуса – в пакете UGENE по схеме Левицкого [25]. Подбор специфичных праймеров и гидролизного (TaqMan) зонда осуществляли с помощью веб-инструмента Primer3 [27]. При разработке олигонуклеотидов соблюдали стандартные критерии, представленные в таблице 1 [28]. Таблица 1 Параметры подбора праймеров и гидролизных (TaqMan) зондов
Специфичность подобранных праймеров и их склонность к образованию димеров дополнительно оценивали in silico с помощью программ Primer BLAST [26] и Multiple Primer Analyzer [28]. Выделение ДНК. Для тестирования эффективности синтезированных олигонуклеотидов в качестве мишени использовали НК клеточной линии FLK. Геномную ДНК выделяли автоматически на станции Nexor 32M с применением набора реагентов для экстракции ДНК/РНК. Количественный анализ полученных нуклеиновых кислот выполняли флуориметрическим методом на анализаторе Qubit 4.0 с использованием высокочувствительного набора SuDye dsDNA HS Assay Kit (Lumiprobe, Россия). Постановка ПЦР в реальном времени. Для оценки эффективности амплификации подобранных праймерных пар была выполнена количественная ПЦР (ПЦР в реальном времени) с использованием разработанных олигонуклеотидов. Реакционная смесь имела следующий состав: экстра-микс HS-Taq (х2) (Диаген, Россия): 100 мМ Трис-HCl, pH 8,5 (При t = + 25°С), 100 мМ KCl, 0,4 мМ каждого дезоксинуклеозидтрифосфата, 4 мМ MgCl2, 0,06 ед. акт./ мкл HS-Taq ДНК-полимеразы, 0,2% Tween 20, стабилизаторы HS-Taq полимеразы, 2 мкл ДНК FLK (54 нг/мкл), 0,3 мМ каждого праймера и зонда, дистиллированная вода до 25 мкл общего объема. Для определения оптимальных условий реакции амплификацию проводили в амплификаторе Bio-Rad CFX96, используя градиент температур на стадии отжига праймеров в соответствии с протоколом, приведенным в таблице 2. Таблица 2 Протокол амплификации с градиентом температуры на этапе отжига праймеров
Для дополнительной валидации способности синтезированных олигонуклеотидов амплифицировать целевой фрагмент, после проведения ПЦР продукты реакции анализировали с помощью горизонтального электрофореза в 3% агарозном геле. Размер ампликонов определяли путем сравнения с ДНК-маркером 1000/10C (diaGene, Россия). Маркер представляет собой набор из 10 фрагментов (от 100 до 1000 п.н.), где фрагмент размером 400 п.н. присутствует в двойной концентрации. Общая концентрация маркера — 0,5 мг/мл. Результаты исследований и их обсуждение. В ходе подбора олигонуклеотидов, комплементарных LTR-региону провируса лейкоза крупного рогатого скота (КРС), были разработаны праймеры и зонд, характеристики которых представлены в таблице 3. Таблица 3 Характеристики праймеров и гидролизного зонда
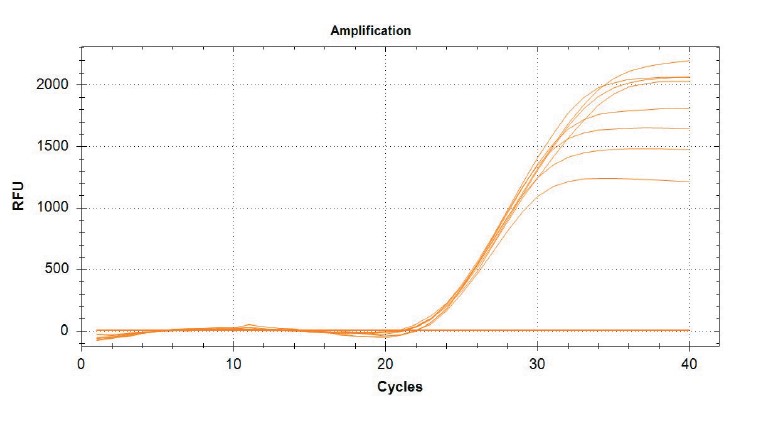
При проведении ПЦР с градиентом температур отжига были зарегистрированы кривые накопления флуоресценции, представленные на рисунке 1. Полученные данные демонстрируют стабильный и высокий уровень сигнала, независимый от конкретной температуры отжига праймеров в заданном диапазоне.
Рис. 1. Кривые амплификации LTR-региона провируса лейкоза КРС с использованием праймеров LTR_177, LTR_374 и зонда LTR_IO_213. ПЦР проводили с градиентом температуры отжига. По оси X – номер цикла амплификации; по оси Y – уровень флуоресценции (RFU) Для оценки специфичности разработанных олигонуклеотидов и контроля образования неспецифических продуктов амплификации был проведен электрофорез продуктов ПЦР в агарозном геле. Электрофореграмма результатов представлена на рисунке 2.
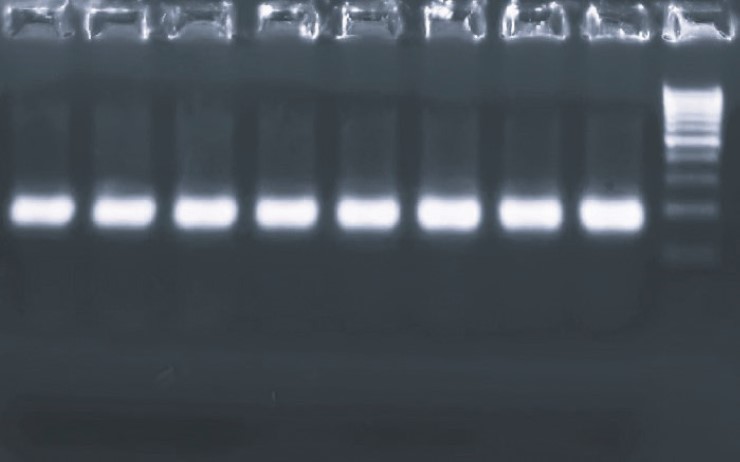
Рис. 2. Анализ продуктов ПЦР методом электрофореза в агарозном геле. Амплификацию LTR-региона провируса лейкоза КРС проводили с праймерами LTR_177, LTR_374 и зондом LTR_IO_213 в режиме градиента температур отжига (дорожки 1-8 – продукты амплификации; М –ДНК-маркер, диапазон 100-1000 п.н., шаг 100 п.н.). В результате проведения ПЦР с градиентом температуры отжига (56-64°C) наблюдалась специфическая амплификация целевого фрагмента размером 198 п.н.; образование неспецифических продуктов не детектировалось. Заключение. В результате проведённого исследования был разработан набор олигонуклеотидов (праймеры и зонд), нацеленный на консервативный участок LTR-региона генома вируса лейкоза крупного рогатого скота, для детекции его провирусной ДНК методом ПЦР в реальном времени. Подбор олигонуклеотидов осуществлён биоинформатическим анализом 200 полногеномных последовательностей ВЛКРС, что обеспечивает теоретическую специфичность системы к широкому кругу циркулирующих изолятов и минимизирует риск ложноотрицательных результатов, связанных с генетической вариабельностью вируса. Экспериментальная проверка на ДНК инфицированной клеточной линии FLK подтвердила функциональную активность системы. ПЦР в режиме градиента температур отжига (56-64°C) продемонстрировала стабильную и эффективную амплификацию целевого фрагмента размером 198 п.н. Отсутствие неспецифических продуктов и праймер-димеров было подтверждено методом электрофореза в агарозном геле. Таким образом, разработанная ПЦР-система является перспективным инструментом для прямого выявления провирусной ДНК ВЛКРС. Её применение позволит повысить точность диагностики на ранних стадиях инфекции, у животных с низкой провирусной нагрузкой, а также в случаях, когда серологические методы малоинформативны (например, у телят с материнскими антителами или иммунотолерантных животных). Целевой дизайн, учитывающий вариабельность ключевых генотипов, направлен на снижение вероятности ложноотрицательных результатов. Для полной валидации метода необходимы дальнейшие исследования по определению его аналитической и диагностической чувствительности, специфичности, а также испытания на расширенной панели клинических образцов. Исследование выполнено за счет гранта Российского научного фонда № 23-16-00103 «Генетическая вариабельность возбудителя и патогенетические особенности течения лейкоза у восприимчивых животных для усовершенствования системы диагностики и ликвидации заболевания». Список литературы: 1. Aida Y., Murakami H., Takahashi M., Takeshima S.N. Mechanisms of pathogenesis induced by bovine leukemia virus as a model for human T-cell leukemia virus. Frontiers in Microbiology. 2013; 4: 328. 2. Burny A., Bex F., Chantrenne H., Cleuter Y. et al. Bovine leukemia virus involvement in enzootic bovine leukosis. Advances in cancer research. 1978; 28: 251-311. 3. Kettmann R., Portetelle D., Mammerickx M., Cleuter Y. et al. Bovine leukemia virus: An exogenous RNA oncogenic virus. Proceedings of the National Academy of Sciences USA. 1976; 73: 1014-1018. 4. Reed V.I. Enzootic bovine leukosis. Canadian Veterinary Journal. 1981; 22: 95-102. 5. Burny A., Bruck C., Cleuter Y., Couez D. et al. Bovine leukaemia virus and enzootic bovine leukosis. Onderstepoort Journal of Veterinary Research. 1985; 52: 133-144. 6. Nekouei O., Vanleeuwen J., Sanchez J., Kelton D., Tiwari A., Keefe G. Herd-level risk factors for infection with bovine leukemia virus in Canadian dairy herds. Preventive Veterinary Medicine. 2015; 119: 105-113. 7. Murakami K., Kobayashi S., Konishi M., Kameyama K., Tsutsui T. Nationwide survey of bovine leukemia virus infection among dairy and beef breeding cattle in Japan from 2009–2011. Journal of Veterinary Medical Science. 2013; 75: 1123. 8. Ma B., Gong Q., Sheng C., Liu Y., Ge G., Li D. et al. Prevalence of bovine leukemia in 1983-2019 in China: A systematic review and meta-analysis. Microbial Pathogenesis. 2021; 150: 104681. 9. Ladronka R.M., Ainsworth S., Wilkins M.J., Norby B. Prevalence of bovine leukemia virus antibodies in US dairy cattle. Veterinary Medicine International. 2018. 5831278. 10. Донник И. М., Петропавловский М. В., Макутина В. А. Современная ситуация по распространению лейкоза крупного рогатого скота в Российской Федерации. Ветеринария. 2024; 11: 18-22. 11. Tsutsui T., Kobayashi S., Hayama Y., Yamamoto T. Fraction of bovine leukemia virus-infected dairy cattle developing enzootic bovine leukosis. Preventive Veterinary Medicine. 2016; 124: 96-101. 12. Gillet N., Florins A., Boxus M., Burteau C. et al. Mechanisms of leukemogenesis induced by bovine leukemia virus: Prospects for novel anti-retroviral therapies in human. Retrovirology. 2007; 4: 18 13. Frie M.C., Coussens P.M., Bovine leukemia virus: A major silent threat to proper immune responses in cattle. Veterinary Immunology and Immunopathology. 2015; 163: 103-114. 14. Nishimori A., Konnai S., Ikebuchi R., Okagawa T., Nakahara A., Murata S., Ohashi K. Direct polymerase chain reaction from blood and tissue samples for rapid diagnosis of bovine leukemia virus infection. Journal of Veterinary Medical Science. 2016; 78: 791-796. 15. Panel E.A. Scientific opinion on enzootic bovine leukosis. EFSA Journal. 2015; 13: 4188. 16. Erskine R., Bartlett P., Byrem T., Render C., Febvay C., Houseman J. Association between bovine leukemia virus, production, and population age in Michigan dairy herds. Journal of Dairy Science. 2012; 95: 727-734. 17. Norby B., Bartlett P., Byrem T., Erskine R. Effect of infection with bovine leukemia virus on milk production in Michigan dairy cows. Journal of Dairy Science. 2016; 99: 2043-2052. 18. Manaa E., Marawan M., Abdelhady A., Selim A. Association between bovine leukemia virus infection, reproductive perfor mance and milk production in water buffaloes and dairy cattle in Egypt. Advances in Animal and Veterinary Sciences. 2020; 8: 1109-1113. 19. Bai L., Yokoyama K., Watanuki S., Ishizaki H., Takeshima S.N., Aida Y. Development of a new recombinant p24 ELISA system for diagnosis of bovine leukemia virus in serum and milk. Archives of Virology. 2019; 164: 201-211. 20. Gutierrez G., Alvarez I., Fondevila N., Politzki R., Lomonaco M. Detection of bovine leukemia virus specific antibodies using recombinant p24-ELISA. Veterinary Microbiology. 2009; 137: 224-234. 21. Kuczewski A., Orsel K., Barkema H.W., Kelton D.F., Hutchins W.A. Short communication: Evaluation of 5 different ELISA for the detection of bovine leukemia virus antibodies. Journal of Dairy Science. 2018; 101: 2433-2437. 22. Endoh D., Mizutani T., Kirisawa R., Maki Y., Saito H., Kon Y., Morikawa S., Hayashi M. Species-independent detection of RNA virus by representational difference analysis using non-ribosomal hexanucleotides for reverse transcription. Nucleic Acids Research. 2005; 33: e65. 23. Pluta A. et al. Inter-laboratory comparison of eleven quantitative or digital PCR assays for detection of proviral bovine leukemia virus in blood samples. BMC Veterinary Research. 2024; Т. 20(1): 381. 24. Tamura K., Stecher G., Kumar S. MEGA11: molecular evolutionary genetics analysis version 11. Molecular biology and evolution. 2021; Т. 38(7): 3022-3027. 25. Okonechnikov K. et al. Unipro UGENE: a unified bioinformatics toolkit. Bioinformatics. 2012; Т. 28 (8): 1166-1167. 26. Untergasser A. et al. Primer3 – new capabilities and interfaces. Nucleic acids research. 2012; Т. 40(15): e115-e115. 27. Rodriguez A. et al. Design of primers and probes for quantitative real-time PCR methods. PCR primer design. 2015: 31-56. Сведения об авторах: Петропавловский Максим Валерьевич, доктор ветеринарных наук, ведущий научный сотрудник ФГБНУ «Уральский федеральный аграрный научно-исследовательский центр Уральского отделения Российской академии наук»; 620142, Свердловская область, г. Екатеринбург, ул. Белинского, 112а; e-mail: petropavlovsky_m@mail.ru. Донник Ирина Михайловна, академик Российской академии наук, доктор биологических наук, профессор, главный научный сотрудник ФГБНУ «Уральский федеральный аграрный научно-исследовательский центр Уральского отделения Российской академии наук»; 620142, Свердловская область, г. Екатеринбург, ул. Белинского, 112а; e-mail: ktqrjp7@yandex.ru. Мартынов Николай Александрович, лаборант ФГБНУ «Уральский федеральный аграрный научно-исследовательский центр Уральского отделения Российской академии наук»; 620142, Свердловская область, г. Екатеринбург, ул. Белинского, 112а; e-mail: martynov_kolya98@mail.ru. Кривоногова Анна Сергеевна, доктор биологических наук, доцент, директор Университетского технологического центра ФГБОУ ВО «Уральский государственный аграрный университет»; 620000, Свердловская область, г. Екатеринбург, ул. Карла Либкнехта, 42; e-mail: tel-89826512934@yandex.ru. Черных Олег Юрьевич, доктор ветеринарных наук, профессор кафедры кафедры микробиологии, эпизоотологии и вирусологии ФГБОУ ВО «Кубанский государственный аграрный университет имени И. Т. Трубилина»; 350044, г. Краснодар, ул. Калинина, 13; e-mail: gukkvl50@kubanvet.ru. Ответственный за переписку с редакцией: Исаева Альбина Геннадьевна, доктор биологических наук, доцент, ведущий научный сотрудник ФГБНУ «Уральский федеральный аграрный научно-исследовательский центр Уральского отделения Российской академии наук»; 620142, Свердловская область, г. Екатеринбург, ул. Белинского, 112а; e-mail: isaeva.05@bk.ru. Заявленный вклад авторов: Петропавловский М.В.: разработка концепции, проведение исследований, формальный анализ, разработка методологии, визуализация, написание рукописи – рецензирование и редактирование. Донник И.М.: разработка концепции, разработка методологии, научное руководство. Исаева А.Г.: курирование данных, формальный анализ, разработка методологии. Мартынов Н.А.: проведение исследования, написание черновика рукописи. Кривоногова А.С.: формальный анализ, визуализация. Черных О.Ю.: курирование данных. Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2011 © Ветеринария Кубани | Разработка сайта - Интернет-Имидж | |
|---|---|---|